© p-a/dpa
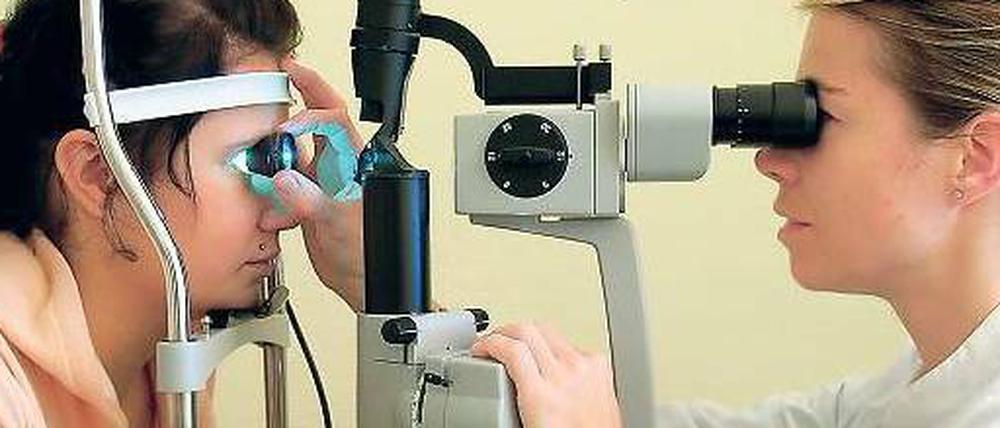
Medizin: Krebsmittel gegen Augenleiden - Streit um Zulassung
Ein preiswertes Krebsmittel hilft auch gegen Erblindung – aber der Hersteller erschwert die Behandlung. Die Apotheker sind durch widersprüchliche Gerichtsurteile verunsichert.
Gute Nachrichten aus der Arzneimittelforschung werden von denen, die im Gesundheitssektor aufs Geld schauen müssen, oft mit zwiespältigen Gefühlen aufgenommen. Schon wieder ein neues Medikament, das zwar ein wenig besser wirkt als die bisher eingesetzten, dafür aber um ein Vielfaches teurer ist. Kein Wunder, wenn die Kosten steigen und steigen! Umso bemerkenswerter, wenn es im Einzelfall anders läuft.
Einen solchen Fall gab es Ende April in der Augenheilkunde bei einer gefürchteten Alterserkrankung: Im Fachblatt „New England Journal of Medicine“ wurden die Ergebnisse der CATT-Studie publiziert, wenige Tage darauf machte auf einem großen amerikanischen Augenärztekongress der dazugehörige Vortrag Furore. Eine Untersuchung des Nationalen Instituts für Augenheilkunde der USA, im Jahr 2008 gestartet, belegte, dass gegen die feuchte Form der altersbedingten Makuladegeneration (AMD, siehe Infokasten) zwei Mittel mit recht unterschiedlichem Preis vergleichbar gut wirken.
Durch die Therapie kann man nicht nur bei den meisten Patienten mit feuchter AMD eine weitere Sehverschlechterung vermeiden, die ohne Therapie fast immer eintritt. Bei vielen Patienten kann man sogar eine nachweisbare Sehverbesserung erzielen. Die Mittel müssen zudem nicht immer, wie bisher vermutet, monatlich gespritzt werden.
Beide Mittel gehören zur Gruppe der VEGF-hemmenden Antikörper, die den Wachstumsfaktor VEGF bremsen und dadurch das krankhafte Aussprossen von Blutgefäßen stoppen. Beide werden direkt in den Glaskörper gespritzt. Das eine, „Lucentis“ (Hersteller Novartis), enthält den Wirkstoff Ranibizumab und ist in Europa seit 2007 für die Behandlung der AMD zugelassen. Das andere, „Avastin“ (Hersteller Roche), enthält den fast identischen Wirkstoff Bevacizumab und wird seit 2004 gegen Krebs eingesetzt.
Seit einigen Jahren ist klar, dass Avastin in deutlich niedrigerer Dosierung auch bei dem Augenleiden wirkt. Und es ist viel preisgünstiger: Für eine Injektion mit Lucentis fällt nach Auskunft der Deutschen Ophthalmologischen Gesellschaft mit 1285,90 Euro ein um das 15- bis 20-fach höherer Apothekenpreis an als für die gleiche Behandlung mit Avastin. Bei mehreren hunderttausend Injektionen pro Jahr ergeben sich erhebliche Einsparmöglichkeiten für die Krankenkassen. Nun ist durch eine große Studie belegt, dass die preisgünstigere Therapie nicht die schlechtere ist. Auch schwerwiegende Nebenwirkungen wie Schlaganfälle und Herzinfarkte, die insgesamt ausgesprochen selten sind, traten beim preisgünstigeren Mittel nicht häufiger auf.
Die Sache hat allerdings einen Haken: Bevacizumab besitzt keine Zulassung für die Behandlung der AMD, sondern nur für einzelne Krebsleiden. Doch die Augenärzte haben durch die CATT-Studie Rückendeckung bekommen und können sich seitdem fachlich auf der sicheren Seite fühlen, wenn sie das preiswertere Mittel spritzen. In einer gemeinsamen Erklärung lassen drei deutsche augenärztliche Fachgesellschaften daran keinen Zweifel: „Die Deutsche Ophthalmologische Gesellschaft, die Retinologische Gesellschaft und der Berufsverband der Augenärzte Deutschlands halten es aufgrund dieser Ergebnisse für notwendig, dass im Sinne der Therapiefreiheit auch die Verwendung des nicht zugelassenen Bevacizumab in der AMD-Therapie innerhalb der gesetzlichen Regelungen möglich ist.“ Im Klartext: Der Augenarzt soll die Freiheit haben, auch das preiswerte Präparat zu spritzen. „Mit der CATT-Studie haben wir viel erreicht“, sagt Georg Eckert, Sprecher des Berufsverbands.
Doch genau das ist ernsthaft infrage gestellt. „Die Ergebnisse der Forschung freuen mich sehr, da ich selbst schon zwölf Spritzen mit Avastin erhalten habe“, schrieb jetzt eine Leserin, die die Berichterstattung im Tagesspiegel aufmerksam verfolgt hatte. Doch sie fährt fort: „Leider musste mir mein Augenarzt vor kurzem mitteilen, dass die Apotheker Avastin nicht mehr in kleinen Dosen an die Augenärzte abgeben dürfen.“
Hier kommt ein technisches Detail ins Spiel: Das für Krebs zugelassene Medikament Avastin ist nur in Packungsgrößen verfügbar, die für die Augenbehandlung deutlich zu groß sind. Lediglich Einrichtungen mit entsprechender Zulassung dürfen Arzneimittel unter strengen Sicherheitsvorkehrungen in kleinere Portionen teilen und in Spritzen aufziehen. Die Augenärzte sind also auf die Apotheken angewiesen.
Die Apotheken sind durch zwei widersprüchliche Gerichtsurteile verunsichert. Nach einer Klage der Herstellerfirma hatte das Oberlandesgericht Hamburg der überregional tätigen Berg-Apotheke mit Sitz im nordrhein-westfälischen Tecklenburg den Vorgang, der in Pharmazeutensprache „Auseinzelung“ genannt wird, untersagt. Das Verbot betraf allerdings interessanterweise nicht Avastin, sondern das für AMD zugelassene Lucentis, das auch in kleineren Mengen eingesetzt wird.
Das Urteil habe wohl keinen Grundsatzcharakter und binde nur die beklagte Apotheke, urteilt der Bund Deutscher Ophthalmologischer Chirurgen. Das Auseinzeln von Lucentis und Avastin und der „Off-Label“-Gebrauch von Avastin bleibe weiter möglich. Dafür spricht, dass das Oberlandesgericht München in einem Urteil die Auseinzelung erlaubt hat.
„Für die Augenärzte besteht eine schwierige Situation, weil sie gern Medikamentenkosten einsparen möchten, dies aber mit Rechtsunsicherheit erkaufen“, sagt Eckert. Genau so sieht das Ursula Sellerberg, Pressesprecherin der Bundesvereinigung Deutscher Apothekerverbände. Bei ihrer Vereinigung gebe es keine Rückmeldung darüber, wie die Apotheker sich tatsächlich verhielten, sagt Sellerberg auf Nachfrage. „Ich fürchte, dass viele es nicht machen, da die Rechtslage uneinheitlich und kompliziert ist und auf die Apotheken auch wirtschaftliche Risiken zukommen.“
Wirkliche Klärung könnte – falls das Problem sich nicht durch eine drastische Preisreduktion für Lucentis erledigen sollte – die Zulassung von Avastin für die AMD bringen, die die Firma Roche beantragen müsste. Auf eine diesbezügliche Anfrage bei der Roche-Anteilseignerin Novartis erhielt der Tagesspiegel die Antwort, man wisse noch zu wenig über mögliche Nebenwirkungen von Bevacizumab, das sich als kompletter Antikörper chemisch von Ranibizumab, dem Fragment eines Antikörpers, unterscheide. „Dieser kleine, aber feine Unterschied im Aufbau der beiden Moleküle kann gravierende Auswirkungen auf das Wohl der Patienten haben“, heißt es aus dem Unternehmen. „Daten aus der Praxis dazu gibt es leider nicht. Denn das Darmkrebsmedikament Avastin ist nicht in der Augenheilkunde zugelassen.“
Hier aber beißt sich die Katze in den Schwanz. Denn eine Überwachung seltener Nebenwirkungen von Medikamenten im großen Maßstab, bei Hunderttausenden von Patienten, ist erst nach deren Zulassung möglich. Die aber hat Roche offenkundig nicht geplant. Würde sie doch dem Anteilseigner Novartis das Geschäft mit dem horrend teuren Lucentis kaputt machen.
- showPaywall:
- false
- isSubscriber:
- false
- isPaid:
- showPaywallPiano:
- false