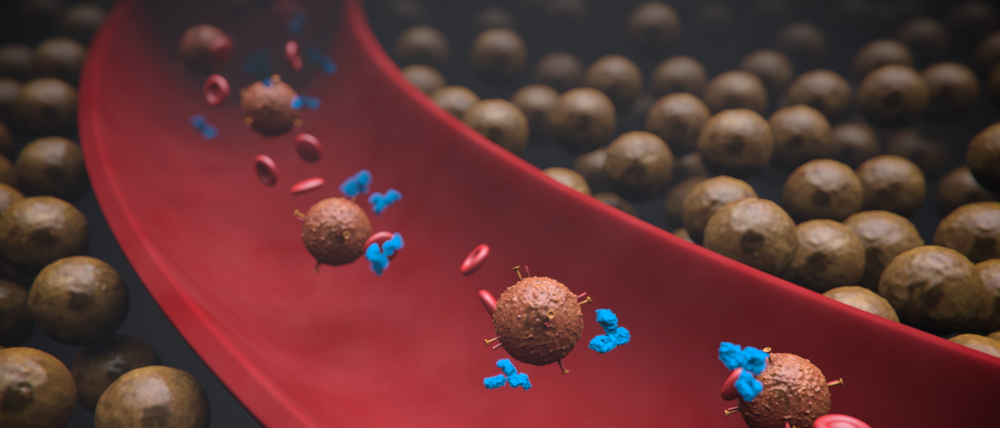
© Illustration: The Netherlands Cancer Institute
Nobelpreis Medizin 2018: Ungehemmte Krebsabwehr
„Checkpoints“ hindern Abwehrzellen, Tumore zu zerstören. Die zwei Nobelpreisträger 2018 haben diese Barriere überwunden und so Selbstheilungskräfte freigesetzt.
Ja, wir können das. Immer wieder und jeden Tag – den Krebs besiegen. Denn im Grunde ist das menschliche Immunsystem in der Lage, Krebszellen von normalen Körperzellen zu unterscheiden und dann gezielt zu zerstören. Entartete Zellen schicken sogar selbstmörderische Notrufe an die Körperabwehr, damit Immunzellen sie finden und zerstören, damit ein ausgewachsener Tumor gar nicht erst entstehen kann. Dennoch gelingt es den Krebszellen mitunter, die Notfallkommunikation zu stören und das Immunsystem auszubremsen.
"Eine Revolution"
Jahrelang erforschte der Biologe James Allison am MD-Anderson-Krebszentrum im texanischen Houston diese Bremsklötze des Immunsystems, „Checkpoints“ genannt, ebenso wie der Japaner Tasuku Honjo an der Universität Kyoto. Beide entwickelten ein völlig neues Therapiekonzept gegen Krebs, das seit einigen Jahren vielen Krebspatienten das Leben rettet, die zuvor als unheilbar galten. Auszeichnungen haben beide Forscher dafür bereits zuhauf und auch gemeinsam bekommen. Jetzt ist die wichtigste Ehrung, die ein Forscher bekommen kann, dazu gekommen: der Nobelpreis für Physiologie oder Medizin. „Was Allison und Honjo entdeckt haben, hat eine Revolution in der Onkologie ausgelöst“, sagt Dirk Jäger, Krebsimmunologe am Deutschen Krebsforschungszentrum in Heidelberg. Die Auszeichnung sei „erwartbar“ gewesen.
Die ersten ernsthaften Tests des Behandlungskonzepts begannen 2001. Zuvor hatten die Forscher Antikörper gegen die Bremsen des Immunsystems entwickelt, Allison gegen den Bremsklotz „CTLA-4“, Honjo gegen „PD-1“. Beides sind Signalmoleküle, die in der Hülle der T-Zellen, wichtiger Abwehrzellen, sitzen. Sie funktionieren ähnlich wie eine Kontrollstelle, ein Checkpoint. Normalerweise lassen sie die Notfallsignale entarteter Zellen passieren, so dass die Körperabwehr aktiviert wird. Doch manche Krebszellen können das verhindern, so dass die Notrufe nicht ankommen und ein Angriff auf die Krebszellen ausbleibt.
Erst todkrank, dann Mutter
Mit ihren Antikörpern gegen die Checkpoints CTLA-4 und PD-1 können Allison und Honjo diese Immunbremsen lösen und die Krebsabwehr reaktivieren. Das gelang zunächst in Laborversuchen, dann auch bei den ersten Patienten. Mit spektakulären Ergebnissen. Wie etwa bei einer damals 26-Jährigen mit so weit fortgeschrittenem schwarzem Hautkrebs, dass bereits die Lunge von Tochtergeschwulsten befallen war und kaum ein Arzt der jungen Frau noch mehr als ein paar Monate Überlebenszeit prognostizieren wollte. Nach nur einer Injektion eines Antikörpers gegen die CTLA-4-Bremse – des inzwischen zugelassenen Wirkstoffs namens Ipilimumab (Yervoy) – löste sich der Krebs buchstäblich auf. „Ein paar Jahre später zeigte sie mir Fotos von ihrem ersten Baby“, berichtete Allison dem Tagesspiegel vor einiger Zeit, als er den Paul-Ehrlich-und-Ludwig-Darmstaedter-Preis verliehen bekam. Es hätte nicht zu diesem oder zum Nobelpreis gelangt, wenn es nach dem Einzelfall seitdem nicht viele weitere Behandlungserfolge gegeben hätte: Jeder fünfte Patient mit fortgeschrittenem schwarzen Hautkrebs wird auf Dauer geheilt. Ähnlich erfolgreich ist das Konzept bei Prostata-, Blasen- und Nierenkrebs.
Alte Idee Immunstimulation
Erstmals in Europa setzten Ärzte der Charité die Checkpoint-Inhibitoren, wie diese Werkzeuge zur Entfesselung des Immunsystems in Fachjargon genannt wird, im Jahr 2006 ein, sagt Ulrich Keilholz, Direktor des Charité Comprehensive Cancer Center. Inzwischen werde etwa ein Drittel der Patienten, etwa tausend pro Jahr, mit Therapien behandelt, die auf Allisons und Honjos Forschungen zurückgehen.
Das Immunsystem gegen Krebs mobil zu machen ist eine Idee, die Ärzte und Biologen schon lange vor Allison und Honjo hatten. 1866 war dem Bonner Chirurgen Wilhelm Busch bereits aufgefallen, dass sich der Krebs bei einer Patientin zurückbildete, nachdem sie sich mit Bakterien infiziert und so ihre Körperabwehr reaktiviert hatte. Später spekulierte auch der Pionier der Immunologie, Paul Ehrlich, dass Krebs im Körper wohl oft entstehe, aber nur ausbreche, wenn das Immunsystem diese „Nester“ nicht mehr bekämpfen könne. Aber Versuche, dieses Wissen in Therapien zu übersetzen, scheiterten immer wieder. „Wir haben lange Zeit immer wieder versucht, das Immunsystem zu stimulieren, aber das hat nie funktioniert“, sagt Keilholz.
Erst gegen Ende des 20. Jahrhunderts verstanden Immunbiologen die feine Regulation des Entfesselns und Abbremsens der Körperabwehr besser. Damit erschloss sich auch, wie das Immunsystem überschießende Reaktionen verhindert, die sich bei bestimmten Erkrankungen auch gegen körpereigene Strukturen richten können. Dies ist etwa bei Multipler Sklerose der Fall. Diese überschießende Reaktion ist allerdings auch eine der gefürchteten Nebenwirkungen der preisgekrönten Krebstherapie. Die Bremse der T-Zellen zu lösen bedeutet eben auch, dass der Körper ein Stück weit die Kontrolle über die Immunreaktion verliert. „Das war am Anfang durchaus immer wieder ein Problem“, sagt Keilholz, inzwischen könne man der Überreaktion aber gezielt entgegenwirken. „Das kommt kaum noch vor.“
Signale für die Abwehr
Inzwischen werden die neuen Therapien meist in Kombination mit den klassischen Behandlungsverfahren, also Operation, Strahlen- und Chemotherapie eingesetzt, sagt Dirk Jäger vom DKFZ. Bei manchen Tumoren, etwa der Lunge, werden sie schon allein und als Ersatz für Chemotherapien angewandt.
Allerdings funktioniert die Therapie längst nicht bei allen Patienten – etwa ein Drittel der mit Checkpoint-Inhibitoren behandelten Patienten mit Schwarzem Hautkrebs spricht darauf nicht an, sagt Keilholz. „Wir müssen bei diesen Patienten erst verstehen, warum sie nicht auf die Behandlung ansprechen“, ergänzt Jäger. Einer der Gründe scheint darin zu liegen, dass Tumoren oft eine Art eigenes „Anti-Immunsystem“ in ihrer direkten Umgebung betreiben, mit Zellen, die die Abwehrreaktion unterdrücken. Jägers Arbeitsgruppe hat eine Signalstoff-Therapie entwickelt, die hier angreift und so Checkpoint-Inhibitoren überhaupt erst Zugang zu Tumoren verschafft. Große Pharma-Unternehmen wie BMS und MSD arbeiteten derzeit an Medikamenten auf dieser Basis, sagt Jäger.
Den Tumor verstehen, um ihn bekämpfen zu können
„Die Balance zwischen Immunreaktion und Tumor-Wachstum ist extrem komplex und im Tumor sind Immunzellen auch hochkomplex reguliert“, ergänzt der Forscher. Je nach Tumorart und Patient könne es hier sehr große Unterschiede geben: „Wir werden in Zukunft Patienten, ihr Immunsystem und ihre Tumoren individuell sehr, sehr viel besser verstehen müssen, um sie zielgenau behandeln zu können, denn wir müssen wissen, welche Mechanismen der Tumor jeweils nutzt.“ Nur so könne man Wege finden, das Immunsystem den Tumor wieder erkennen und angreifen zu lassen.
Kombinationen der neuen Therapien können in Zukunft vielleicht noch mehr Menschen helfen. Für jene etwa, die auf Allisons Antikörper Ipilimumab allein nicht reagierten, könne man zusätzlich eine andere Therapie einsetzen, sagt Lars Bullinger, Tumorimmunologe an der Charité. Bezeichnenderweise ist ein solcher Ansatz die Kombination mit Antikörpern gegen PD-1. Es ist also eine Therapie, die die Befunde Allisons und Honjos zusammenführt.
Ein großes Problem ist derzeit, wie fast immer, das Geld. Die Kosten seien „zu hoch“, sagt Ulrich Keilholz. „Anfangs hatten die Pharmafirmen nur mit etwa 5000 Patienten in Deutschland gerechnet, den Preis also entsprechend einer Nischenindikation kalkuliert.“ Doch inzwischen seien es allein in Deutschland sicher 50.000 pro Jahr, die mit Ipilimumab und ähnlichen Wirkstoffen behandelt würden. Die Herstellungskosten fallen zu wenig ins Gewicht, als dass die Kalkulation nicht angepasst werden könnte, sagt Keilholz: „Es ist an der Zeit.“

© REUTERS
- showPaywall:
- false
- isSubscriber:
- false
- isPaid:
- showPaywallPiano:
- false