© Biozentrum, Uni Basel, xxpool
Die Antibiotika-Krise, Teil 4: Die Bakterienfresser
Bakterien sind winzig. Aber sie sind nicht winzig genug, um selbst einer Infektion zu entgehen. Viren, die Bakterien befallen, gelten als einer der Hoffnungsträger im Kampf gegen multiresistente Keime.
Stand:
Bakterien sind Täter. Sie fallen über Menschen her, dringen ins Blut und in Organe ein und überfrachten geschwächte Patienten mit tödlichen Giften. Ab 2050 könnten solche Infektionen zusätzlich zehn Millionen Menschen pro Jahr töten, schätzt eine vom britischen Premierminister David Cameron eingesetzte Kommission. Denn immer mehr Mikroben werden resistent gegen Antibiotika. In dieser Situation suchen Forscher dringend nach neuen Strategien für die Behandlung – und erinnern sich an eine hundert Jahre alte Entdeckung: Bakterien sind nicht nur Täter, sondern auch Opfer. Von Viren.
Seit Jahrmilliarden werden Bakterien von ihren ganz eigenen Parasiten befallen: „Bakterienfressern“ (Bakteriophagen), Viren, die ausschließlich Bakterien infizieren. Sie spritzen ihr Erbgut durch die Hülle der Bakterienzelle und zwingen sie, neue Phagen zu produzieren, bis die Zelle daran stirbt. Im Stuhl von Durchfallpatienten beispielsweise treten immer dann zahlreiche Bakterienfresser auf, wenn diese sich gerade von einer Infektion mit Shigellen-Bakterien erholen, beobachtete 1917 der britisch-kanadische Mikrobiologe Felix d’Hérelle vom Pariser Pasteur-Institut. Sollten die Bakterienfresser dafür verantwortlich sein?
Sein Kollege George Eliava, ein georgischer Arzt, war der Erste, der die Phagen systematisch zur Behandlung einsetzte. In Tiflis gründete er 1923 ein Institut. Dort und in anderen Ländern, die einst zur Sowjetunion gehörten, werden bis heute Cocktails verschiedener Bakteriophagen gegen bakterielle Infektionen verabreicht. Im Westen hingegen geriet die „Phagentherapie“ in Vergessenheit, nachdem in den 1940er Jahren die Antibiotika auf den Markt kamen.
Nützliche Darmbakterien werden verschont
Inzwischen ist das Interesse an den Phagen weltweit groß. Das Nationale Institut für Allergien und Infektionskrankheiten der USA (NIAID) listet die Phagentherapie als eine der aussichtsreichsten Strategien gegen resistente Bakterien. Mit 3,8 Millionen Euro finanziert die Europäische Kommission das „Phagoburn“-Programm. Es ist die erste größere Studie in der EU, die an etwa 220 Patienten untersuchen wird, wie wirksam die Phagen gegen Infektionen mit schwer behandelbaren Darmbakterien wie Escherichia coli und Pseudomonas aeruginosa sind. Die Patienten bekommen einen Mix aus einem Dutzend verschiedener Viren. Damit soll die Wahrscheinlichkeit reduziert werden, dass ein Bakterium zufällig gegen die Viren resistent wird – zum Beispiel indem es die Andockstellen für die Phagen auf der Zellmembran ändert oder verschwinden lässt.
Ein Vorteil der „Phagentherapie“ ist, dass die Viren auf einzelne Bakterienarten spezialisiert sind. Nützliche Darmbakterien werden so ausgespart. Die Viren können sogar speziell gegen resistente Bakterien vorgehen. Timothy Lu vom Massachusetts Institut of Technology in Cambridge veränderte das Erbgut von Bakteriophagen kürzlich so, dass sie eine „molekulare Genschere“ in die Bakterien schleusen. Die Schere erkennt und zerschneidet nur jene Gene, die ein Bakterium vor Antibiotika schützen. Die Bakterien bleiben am Leben, sind aber fortan empfindlich gegen die Medikamente.
Resistente Erreger werden wieder empfindlich gegen Antibiotika
„Resistente Krankheitserreger sind eine wachsende Gefahr. Der Einsatz von Antibiotika führt dazu, dass sie gegenüber den empfindlichen Bakterien einen Vorteil haben“, sagt Udi Qimron von der Universität Tel Aviv. Er will gentechnisch frisierte Bakteriophagen in Desinfektionssprays in Krankenhäusern einsetzen. Bisherige Mittel töten zwar viele, aber nie alle Bakterien und mitunter sind gerade die überlebenden Mikroben resistent. Deshalb hat Qimron ein Phagen-Spray entwickelt, dass nicht nur Bakterien abtötet, sondern dafür sorgen soll, dass nur noch die „richtigen“, die für Antibiotika empfindlichen Bakterien auf Türklinken, Tischen, Smartphones und Händen von Ärzten überleben. „Unsere Strategie ist insofern einzigartig, als sie resistente Bakterien wieder empfindlich gegen Antibiotika macht“, sagt Qimron.
Die Phagen sind wie ein Trojanisches Pferd
Dazu nutzt er nacheinander zwei verschiedene Phagen-Typen (siehe Grafik): Einen scheinbar harmlosen, der in möglichst viele Bakterienzellen die Erbinformation für eine „molekulare Genschere“ schleust, die Resistenzgene zerschneiden kann. Infiziert der Phage also ein resistentes Bakterium, werden diese Gene zerstört. In Bakterien ohne diese Resistenzgene hat die Schere zunächst nichts zu tun – doch sie hat noch eine zweite Funktion: Sie schützt auch vor Killerphagen, die Qimron in einem zweiten Schritt einsetzt und deren Erbgut die Schere erkennt und zerschneidet.
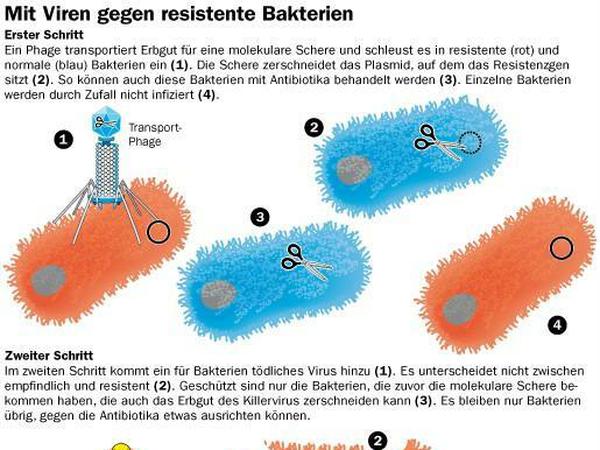
© Anna Schmidt
Bakterien mit molekularer Schere haben also plötzlich einen Überlebensvorteil, also jene Mikroben, die später mit Antibiotika behandelt werden können. Die Taktik funktioniere wie ein Trojanisches Pferd, sagt Qimron. „Die Bakterien empfangen die molekulare Schere als Geschenk. Aber später, wenn Antibiotika eingesetzt werden, werden sie abgetötet.“ Bevor das Phagenspray in Krankenhäusern eingesetzt werden kann, will es Qimron aber erst in Mäusekäfigen testen.
Die Phagen sind nicht die einzigen Hoffnungsträger, mit denen künftig resistente Bakterien bekämpft werden sollen. Aufsehen erregte kürzlich die Entdeckung des Wirkstoffes Teixobactin – nicht nur, weil die Substanz diverse resistente Bakterienstämme abtötet. Vielmehr gelang es Tanja Schneider vom Deutschen Infektionszentrum in Bonn und Kim Lewis und Slava Epstein von der Northeastern University in Boston die Boden-Bakterien im Labor zu züchten, aus denen der Stoff stammt. Zwar wissen Forscher seit Langem, dass sich Bakterienarten gegenseitig mit einer Fülle von Stoffen bekämpfen, die als Antibiotika taugen würden. Doch nur wer die Bakterien im Labor halten kann, kann mit ihrer Hilfe auch neue Wirkstoffe gewinnen.
Silber und Kupfer wurde bereits in der Antike zur Desinfektion eingesetzt
Den Forschern mangelt es nicht an Ideen, woher neue Antibiotika kommen könnten. Manche setzen auf Altbekanntes, wie die Bakterienfresser oder Metalle wie Silber und Kupfer, die schon in der Antike zur Desinfektion eingesetzt wurden. Neueren Datums ist die Beobachtung, dass Amphibien und Reptilien aufgrund spezieller kurzer Eiweiße (Peptide) besonders widerstandsfähig gegen Infektionen sind. Pexiganan, ein Peptid eines Krallenfroschs, durchläuft derzeit die letzte klinische Prüfphase. Wieder andere Forscher versuchen, die Mechanismen zu blockieren, mit denen Bakterien Antibiotika entgehen.
Mit Antibiotika kann man nichts verdienen, heißt es
Aber viele der schönen neuen Ideen schaffen es nicht, zum fertigen Medikament zu reifen. Denn spätestens seit der Jahrtausendwende machen Pharmafirmen um diese Forschung einen Bogen. Mit Antibiotika ist kaum Geld zu verdienen, heißt es. Denn die meisten Infektionen in den Industrieländern können (noch) mit den gängigen, sehr billigen Antibiotika behandelt werden; neue Mittel werden zum Ladenhüter. Außerdem halten Ärzte die wenigen, gegen multiresistente Erreger wirksamen Stoffe zurück und verwenden sie nur im Notfall. Sie wollen den Bakterien keine Gelegenheit geben, diese letzten Waffen stumpf werden zu lassen. Wenn sie sie einsetzen, dann nur kurzzeitig – jedenfalls im Vergleich zu Medikamenten gegen Krebs oder chronische Erkrankungen. All das hemmt Investitionen in neue Antibiotikakonzepte.
Inzwischen versucht die Politik, den Arzneimittelherstellern das Antibiotikageschäft wieder schmackhaft zu machen. In den USA hilft beispielsweise das „Gain“-Gesetz (Generating Antibiotic Incentives Now) seit 2012 dabei, dass neuartige Antibiotika schneller zugelassen werden und der Patentschutz fünf Jahre länger als üblich gewährt wird. Die vom britischen Premier eingesetzte Kommission schlägt vor, dass ein international finanziertes Organ den Firmen Prämien von bis zu drei Milliarden Dollar zahlen soll, wenn sie ein neues Antibiotikum auf den Markt bringen und vorhalten. Einen solchen Forschungsfonds der G-7-Staaten unter Führung der Weltgesundheitsorganisation WHO fordern auch „Ärzte ohne Grenzen“ und einflussreiche Forscher im Fachblatt „Plos“. Allerdings solle solch ein Topf neben Antibiotika- auch Impfstoff- und Medikamentenentwicklungen gegen weltweit vernachlässigte Krankheiten finanzieren.
Die Bakterien müssen nicht unbedingt getötet werden
Das Umdenken trägt anscheinend Früchte, immerhin investieren Konzerne wie Roche seit 2013 wieder in die Antibiotikaforschung. Die US-Pharmafirma Merck & Co. (MSD) hat kürzlich 8,5 Milliarden Dollar ausgegeben, um die US-Firma Cubist zu übernehmen, die seit 1992 neue Antibiotika wie Cubicin entwickelt. Der Wirkstoff durchlöchert die Bakterienmembran und wirkt sogar dann noch gegen multiresistente Staphylokokken-Bakterien (MRSA), wenn Reserveantibiotika wie Vancomycin versagen. Entgegen der Einschätzung, Antibiotikaentwicklung lohne sich nicht, machte Cubist damit jährlich einen Umsatz von rund einer Milliarde Dollar. Ende letzten Jahres ließ die amerikanische Zulassungsbehörde FDA außerdem das Mittel Zerbaxa zu. Es kombiniert zwei Wirkstoffe, von denen einer das Enzym Beta-Lactamase lahmlegt, mit dem resistente Escherichia coli-Darmbakterien Antibiotika unschädlich machen.
Weitere Wirkstoffe in der Entwicklung versuchen den Bakterien auf anderen Wegen zuzusetzen. Dabei muss es nicht immer das Ziel sein, die Bakterien zu töten, sagt MSD-Antibiotika-Experte Barry Eisenstein, seit 2003 bei Cubist und an der Beth-Israel-Klinik der Harvard-Universität. „Wir versuchen, die zwei wichtigsten Gifte, die der Darmkeim Clostridium difficile produziert, mit Antikörpern abzufangen.“ Das wirke sich positiv auf die gefährliche Durchfallerkrankung aus, die Clostridien auslösen.
Bakterienfresser zu Antibiotika zu entwickeln, plant MSD vorerst nicht, obwohl Eisenstein die Phagentherapie für ein interessantes Konzept und Qimrons Strategie für „sehr clever“ hält. „Ich bin gespannt, wie sie sich in Tests bewähren wird.“ Die eine ideale Lösung gegen antibiotikaresistente Bakterien werde es ohnehin nicht geben. Um den resistenten Mikroben künftig immer einen Schritt voraus zu sein, müsse es eine Fülle neuer Antibiotika geben.
- showPaywall:
- false
- isSubscriber:
- false
- isPaid: