© Yueheng Zhou, Absea Biotechnology und Mohsen Sadeghi, Freie Universität Berlin
Gut Getarnt: Wie sich ein Herpesvirus in der Zelle versteckt
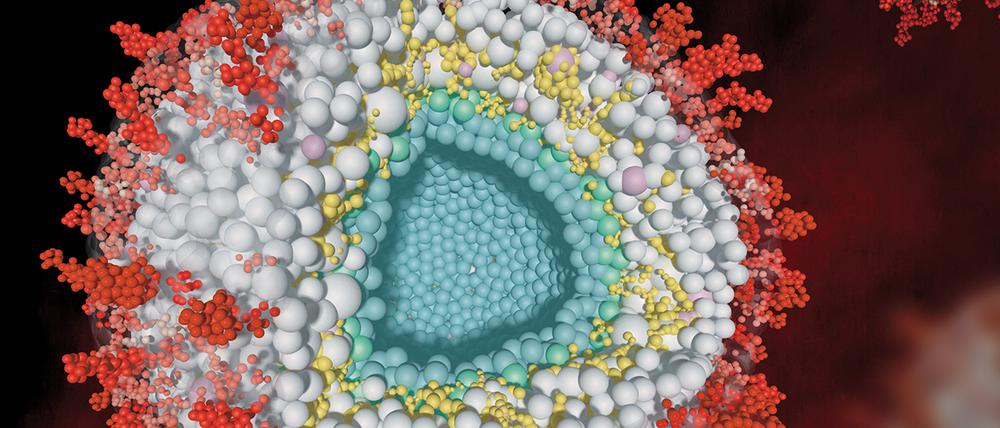
Eingehüllt in Bestandteile der Wirtszelle überdauern Herpesviren die Attacken des Immunsystems. Berliner Forschende haben nun erstmals einen solchen Viruspartikel modelliert.
Stand:
Einmal infiziert, immer infiziert: Wer sich einmal ein Herpesvirus einfängt, wird es nie wieder los, denn der Erreger schafft es, sich gegen das Immunsystem seines Wirtes abzuschirmen. Dafür integriert er offenbar gezielt Eiweiße der Wirtszelle in seinen Bauplan.
Damit kann das Virus der infizierten Zelle vortäuschen, dass sie gar nicht infiziert oder bedroht ist, erklärt ein Berliner Forschungsteam im Fachmagazin „Nature Microbiology“, das sich den Aufbau des humanen Cytomegalievirus genauer ansah. Dieses Virus zählt zu den Herpesviren, auch wenn es keine der berüchtigten Lippenbläschen verursacht.
Stattdessen verläuft eine Infektion häufig unbemerkt. Bei Personen mit eingeschränkter Immunfunktion wie Aids-Patient:innen kann sie jedoch lebensbedrohlich werden. Bei einer Übertragung von der infizierten Mutter auf das Ungeborene kann das Virus zu einer Behinderung des Kindes oder Gehörverlust führen.
„Wir haben das allererste grobstrukturierte Modell nicht nur für das Cytomegalievirus, sondern für Herpesviren im Allgemeinen erstellt“, sagt Fan Liu vom Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP), eine der Studienleiterinnen. Zusammen mit Teams von Charité und Freier Universität hat sie den Aufbau der Virus-Partikel in vereinfachter Form virtuell simuliert.
Vielschichtiges Problem
Das Virusmodell erinnert an eine haarige Mozartkugel mit vier Schichten. Ganz im Inneren befindet sich das Erbgut, umschlossen von einer Kapsel. Von beiden ist der Aufbau längst bekannt. Knapp unter der Außenhülle aus Zucker und Fett tummelt sich ein Mix aus viralen und humanen Eiweißen, deren räumliche Organisation das Berliner Team nun erstmals kartiert hat. Dabei stellte sich heraus, dass das Virus gezielt Enzyme des Phosphat-Stoffwechsels seines Wirtes anzieht und sich mit ihrer Hilfe effizienter vermehren kann.
Um ihren räumlichen Aufbau zu entschlüsseln, hatten die Forschenden Viren in der Zellkultur vermehrt und anschließend mit einer Chemikalie behandelt, die benachbarte Eiweißbestandteile untereinander verknüpft. Die durch dieses „crosslinking“ verklumpten Proteine schickten die Forschenden anschließend durch ein Massenspektrometer, das die Molekülmassen misst. So identifizierten sie die jeweiligen Nachbarn eines jeden Proteins und wie stark sie aneinander haften, erklärt Fan Liu. Auf diesen biophysikalischen Messwerten wiederum baute die digitale Simulation auf.
Wettlauf gegen neue Varianten
Praktisch jeder Erwachsene trägt mindestens eines der neun verschiedenen humanen Herpesviren in sich, ohne es zu wissen. Durch Alter, Stress oder eine Abwehrschwäche kann das Virus reaktiviert werden. Die getarnten Partikel in der Zelle spielen dabei eine bedeutende Rolle. Eine Cytomegalie verläuft jedoch meist mild und es gibt einige Medikamente, die den Erreger hemmen. Wozu also noch weiter daran forschen?
„Die Covid-Pandemie hat uns daran erinnert, dass Viren neue Varianten entwickeln können, die gegen bestehende Therapeutika oder Impfstoffe resistent sind“, erklärt die Forscherin auf Nachfrage. Dies sei beim Cytomegalievirus nicht anders, bereits jetzt gebe es Varianten, die auf gängige Medikamente nicht ansprächen: „Wir müssen alternative Virostatika entwickeln, die das Virus auf andere Weise bekämpfen.“
Neben klassischen virushemmenden Medikamenten existieren Antikörper-Präparate, womit Transplantat-Empfänger:innen oder infizierte Schwangere vorsorglich behandelt werden. Aber für die Anwendung in werdenden Müttern gibt es keine offizielle Zulassung, ein Streit um die Kostenerstattung kommt nun sogar vor das Bundesverfassungsgericht.
Für neue, wirksame Medikamente gibt es also einen Bedarf. Auch an Impfstoffen wird seit Jahrzehnten geforscht, allerdings weitgehend erfolglos. Kürzlich jedoch hat das US-Unternehmen Moderna eine Vakzine entwickelt, die nach einem ähnlichen Prinzip funktioniert wie der Corona-Impfstoff auf RNA-Basis. Der Konzern vermeldete 2021 vielversprechende Zwischenergebnisse. Jetzt strebt er umfangreiche klinische Studien mit einigen tausend Teilnehmerinnen an.
- showPaywall:
- false
- isSubscriber:
- false
- isPaid: